Помутнело в глазах. Как выявить глаукому на ранней стадии
Глаукома — лидер среди причин инвалидности по зрению. Терминальная стадия заболевания приводит к полной слепоте. Бытует ложное мнение, что глаукома атакует только пожилых, но на самом деле ее жертвами становятся и 35—40-летние. Зачастую болезнь протекает бессимптомно, поэтому многие пациенты не знают о ней и не обращаются к врачам. Рассказываем о новейших методах диагностики и лечения глаукомы, а также о том, из-за чего она возникает.
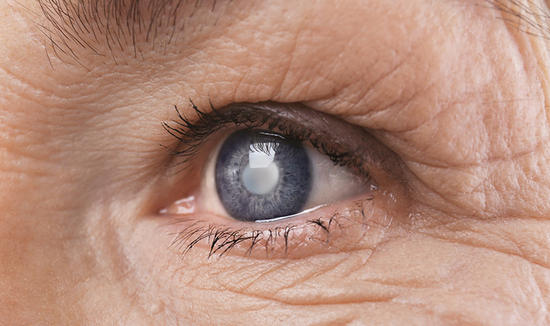
Заболевание с запоздалой диагностикой
Глаукома — группа офтальмологических заболеваний, которым свойственна прогрессирующая дегенерация зрительного нерва с потерей ганглиозных клеток сетчатки. Эти клетки обрабатывают сигналы, получаемые от фоторецепторов, и передают через зрительный нерв в мозг.
Самая распространенная форма болезни — открытоугольная глаукома. Как правило, вначале она протекает бессимптомно. В некоторых случаях возникают неспецифические симптомы — периодическое затуманивание зрения, мерцающая скотома, боль в глазах, цефалгия. На терминальной стадии глаукомного процесса наступает необратимая слепота.
Доклиническая и начальная стадии заболевания длятся от года до пяти лет. Случается, что болезнь развивается очень стремительно и через 3–5 лет после ее манифестации человек полностью лишается зрения.
В России на начало 2022 года было зарегистрировано почти четверть миллиона пациентов с глаукомой. Жертвами заболевания становятся люди в возрасте от 35 до 90 лет.
В 40–80% случаев глаукома диагностируется на поздних стадиях, когда предотвратить потерю зрения уже невозможно.Половину случаев слепоты, связанной с глаукомным процессом, можно избежать при своевременной диагностике. Запоздалая диагностика болезни связана с длительным отсутствием симптомов и сложностями выявления ее на начальной стадии. В России всем гражданам, достигшим 40-летнего возраста, во время ежегодной диспансеризации проводится тонометрия — измерение внутриглазного давления (офтальмотонуса). И хотя его повышение относится к распространенным признакам глаукомы, для выявления заболевания результатов тонометрии бывает недостаточно. Около 47% пациентов с глаукомой имеют нормальное внутриглазное давление. Это означает, что точность тонометрии составляет примерно 53%.
Факторы риска
К факторам риска глаукомы относятся возраст и наследственная предрасположенность. Около половины пациентов с глаукомой имеют положительный семейный анамнез, а у их родственников первой линии вероятность развития заболевания повышена в 9 раз.
На вероятность развития глаукомы влияют врожденные особенности роговичной оболочки глаза: чем она тоньше, чем выше риск заболевания.
Мощный провокатор глаукомы — миопия (близорукость), которая встречается примерно у каждого десятого ребенка и четверти взрослых. При низкой степени близорукости риск глаукомы повышен в 1,77 раза, при высокой — в 2,46 раза.При близорукости увеличивается длина глаза, что приводит к повышению внутриглазного давления и снижению биомеханических свойств роговицы. Кроме того, при миопии часто развивается синдром пигментной дисперсии, при котором пигментные клетки отделяются от радужной оболочки. В свою очередь, этот синдром в 25–50% случаев приводит к развитию пигментной глаукомы. При близорукости она чаще всего возникает в возрасте 30–50 лет.
Вероятность глаукомного процесса возрастает при высоком артериальном давлении: у 48–65 % пациентов с первичной открытоугольной глаукомой диагностируется гипертоническая болезнь. При высоком АД увеличивается продукция внутриглазной жидкости и нарушается ее отток, что способствует повышению офтальмотонуса.
У пациентов с сахарным диабетом 2-го типа глаукома встречается в 4–5 раз чаще, чем у людей без него. Риск развития глаукомы повышается при стаже диабета 12–15 лет и более, наличии диабетической ретинопатии, отсутствии компенсации заболевания. Применение метформина коррелирует со снижением риска глаукомы.
При СД 2, особенно декомпенсированном, развивается эндотелиальная дисфункция, приводящая к выработке тканями провоспалительных цитокинов. Воспаление участвует и в патогенезе глаукомы. При гипергликемии нарушается отток жидкости из глаза и поддержание нормального внутриглазного давления, а также увеличивается риск ретинопатии, которая провоцирует глаукому.
У крыс с индуцированным СД наблюдается истончение ганглиозных клеток. Уже через 12 недель после индукции диабета у них уменьшается толщина миелиновой оболочки и площадь нервного пучка зрительного нерва. Все эти процессы свойственны глаукомному процессу.
Предполагается, что глаукома может быть связана с болезнью Альцгеймера (БА). Первичная открытоугольная глаукома диагностируется почти у половины людей с альцгеймеровской деменцией. Базовая теория возникновения БА — отложение β-амилоида в головном мозге. Сегодня доказано, что β-амилоид участвует и в разрушении ганглиозных клеток при глаукоме.
Подводные камни тонометрии
К базовым методикам диагностики глаукомы относится тонометрия, которую проводят разными способами. В России распространены тонометрия по Маклакову, по Гольдману и пневмотонометрия. Ни одна из этих методик не учитывает в достаточной мере индивидуальные особенности фиброзной оболочки глаза, что приводит к неточной диагностике.
Биомеханические свойства фиброзной оболочки, включая ее толщину, влияют на точность измерения внутриглазного давления. Тонкая роговица может приводить к недооценке результатов тонометрии, толстая — к переоценке.
Избежать подобных ошибок позволяет применение анализатора глазных реакций ORA, динамического контурного тонометра Pascal и аппарата iCare.Прибор ORA определяет центральную толщину, вязкоэластичные, упругие свойства роговицы и другие параметры, влияющие на внутриглазное давление. Учет этих показателей имеет первостепенное значение при измерении внутриглазного давления у людей с близорукостью, при которой изменяются биомеханические свойства роговицы.
Нередко результаты тонометрии становятся основанием для постановки диагноза «глаукома», а после оказывается, что этой болезни у человека нет. Некоторые офтальмологи после однократно зафиксированного высокого внутриглазного давления начинают подозревать у пациента глаукомный процесс и назначают гипотензивные препараты, хотя повышение офтальмотонуса, тем более эпизодическое, далеко не всегда указывает на наличие глаукомы. У 4–10% взрослых старше 40 лет тонометрия фиксирует высокое внутриглазное давление, однако у 90% из них глаукома не возникает.
В клинических рекомендациях подчеркивается, что внутриглазное давление должно оцениваться в динамике. Кроме того, для постановки диагноза «глаукома» результатов только тонометрии недостаточно.
Ученые хабаровской глазной клиники провели комплексное обследование 30 пациентов, которым был поставлен диагноз «глаукома» и назначены гипотензивные препараты. Только у шести пациентов диагноз был верным. У остальных испытуемых глаукому не обнаружили, и гипотензивные препараты им были не нужны.
Назначение гипотензивного лечения без наличия показаний приводит к возникновению синдрома «сухого глаза» и ухудшению качества жизни, вплоть до развития системных осложнений.

Комплексный подход к диагностике
На сегодняшний день не существует какой-либо универсальной методики диагностики начальной стадии глаукомного процесса. Способов выявления его признаков много, но самым достоверным является обследование, состоящее из тонометрии, периметрии и офтальмоскопии.
Компьютерная периметрия применяется для исследования границ поля зрения.
Две последовательно проведенные периметрии позволяют диагностировать начальную стадию глаукомного процесса в 97% случаев.Периметрия рекомендована и для мониторинга прогрессирования заболевания. В современных клинических исследованиях именно ее результаты используются для выбора тактики лечения.
Офтальмоскопия — исследование глазного дна для оценки состояния диска зрительного нерва, толщины слоя нервных волокон сетчатки и других показателей. Эффективность методики повышается, если после нее проводится оптическая когерентная томография (ОКТ). С помощью этого исследования можно перевести информацию, полученную при офтальмоскопии, в конкретные цифры.
Сегодня ОКТ признана «лидером» среди инструментальных технологий визуализации глазного дна. Она позволяет рассмотреть структуру ткани сетчатки с разрешением от 1 до 15 микрон, что значительно выше разрешающей способности УЗИ, МРТ и КТ. При проведении ОКТ-ангиографии можно исследовать мельчайшие сосуды, вплоть до капилляров в разных областях сетчатки и на разной глубине. Многими клиническими исследованиями доказана высокая эффективность ОКТ как в диагностике ранних стадий глаукомы, так и в динамическом наблюдении за ее течением.
Многоцентровое международное исследование, проводимое в странах СНГ (включая Россию) и Восточной Европы, продемонстрировало, что в период с 2005 по 2020 год подход к диагностике глаукомы стал более комплексным. Во всех офтальмологических клиниках, принимавших участие в исследовании, при диагностике глаукомы используется офтальмоскопия. Оптическая когерентная томография применяется в 90% клиник, периметрия — в 95%.
Слабая сторона диагностики глаукомы — широкая распространенность устаревших методов тонометрии. В частности, в России тонометрия по Маклакову остается «золотым стандартом». Тонометрия с регистрацией биомеханических параметров роговицы используется крайне редко.
Лечение
Повышенный офтальмотонус — единственный фактор, на который можно воздействовать при глаукоме. Нормализация внутриглазного давления может осуществляться с помощью фармакотерапии, лазерного лечения, оперативного вмешательства.
Как правило, медикаментозное лечение начинается с монотерапии аналогами простагландинов, которые улучшают отток жидкости из глаза и способствуют снижению внутриглазного давления. Если эта схема не работает, назначается терапия несколькими гипотензивными средствами либо применяется фиксированная комбинация (ФК) — готовый лекарственный препарат, содержащий два и более действующих вещества. ФК упрощает режим закапываний, снижает риск вымывания лекарственных средств из глаза, повышает лечебный эффект.
При неэффективности медикаментозной терапии применяются хирургические методы лечения глаукомы, включая лазерные. Последние имеют ряд преимуществ перед операцией — низкий риск осложнений, отсутствие необходимости в госпитализации, возможность лечения пациентов с сопутствующими заболеваниями, при которых хирургия противопоказана. Лазерные методики используются для лечения так называемой «рефрактерной глаукомы» — невосприимчивой к стандартным лечебным методикам.
Долгое время для лечения глаукомы применялась транссклеральная ЦФК — по некоторым параметрам она превосходила оперативное вмешательство, но зачастую приводила к воспалительным процессам, ухудшению зрения, отслойке сосудистой оболочки глаза. Это послужило толчком для разработки новой, более безопасной методики — микроимпульсной ЦФК (мЦФК). С 2018 года она применяется и в России. мЦФК позволяет дозированно воздействовать на сосудистую оболочку глаза, что защищает ее от перегрева и разрушения.
Команда российских ученых оценила состояние 56 пациентов с прогрессирующей глаукомой, прооперированных методом мЦФК.
После операции ни у одного пациента не возникло осложнений. Снижение внутриглазного давления наблюдалось уже в первый день после оперативного вмешательства, через полгода после него в 94% прооперированных глазах уровень офтальмотонуса соответствовал норме.Исследователи сделали вывод: мЦФК — атравматичная и эффективная методика лечения прогрессирующей глаукомы, дающая пролонгированный лечебный эффект и позволяющая сохранить зрительные функции.
Смягчает течение глаукомы биологическая обратная связь (БОС) — поведенческая терапия, которая учит управлять различными физиологическими параметрами. Во время процедуры на теле фиксируют датчики, которые определяют те или иные показатели работы организма и выводят их на монитор. Опираясь на полученную информацию, человек учится управлять ими.
При начальной стадии глаукомы показывают эффективность БОС-тренинги по электрическому сопротивлению кожи, которые избавляют пациентов от дискомфорта в глазах, слезотечения, головных болей. Они способны улучшать зрительные функции (сокращать площадь слепого пятна, увеличивать поле зрения). При сочетании БОС с медикаментозным лечением внутриглазное давление нормализуется быстрее, чем при использовании только гипотензивных препаратов.









Комментарии
Отойдя от темы зрения, хочется затронуть комплексно медицину в Эстонии, что ничего здесь обычный человек получить не сможет. На примере собственной семьи. У мужа два года назад началась ужасная непроходящая диарея. За месяц он потерял 12 килограмм. На протяжении трёх месяцев потеря веса составила 24 килограмма. За всё это время мы от семейного врача добились только курса антибиотиков, анализы крови и УЗИ. Больше ничего. Врача даже не смутили низкие показатели крови и железа. Направления на КТ, на колоноскопию мы не смогли получить. Врач лишь говорил, не накручивайте себя, всё от нервов и дала направление супругу к неврологу. Когда ничего не помогло, семейный врач всё же направила мужа на колоноскопию, но оказалось, что врач в отпуске и ближайшая запись через два месяца. К тому времени муж похудел уже на 27 килограмм! Диарея с выходом огромного количества жидкости продолжалась. Слабость, утомляемость, потеря аппетита. Больше ждать не было возможности. Я связалась с сестрой, которая живёт в Санкт-Петербурге и мы поехали туда на платное обследование. Консультация бесплатно. Мужа сразу положили на стационар, прокапали, когда показатели крови вышли на норму, сделали КТ с контрастом и колоноскопию. Результат: рак прямой кишки, 3 стадия. Мы вернулись в Эстонию, но здесь результаты анализов из России приняты не были и семейный врач продолжал настаивать на том, что мы должны дождаться своей очереди на колоноскопию здесь. Но всё же выписала направление к онкологу в Тарту. Запись 3 месяца! Мы продали машину, я взяла кредит и мы вернулись в Россию на лечение. Курсы химиотерапии, опухоль хорошо среагировала на химию и мужа положили на операцию. Сейчас болезнь ушла в ремиссию. Супруг живой. На обследования ездит только в Питер теперь к нашему лечащему врачу. А наш здесь неуважаемый семейный врач продолжает заниматься прививками пенсионеров и экономией денег на здоровье людей.
вот видите какой бардак устроили в ЕС...
Бардак, некомпетентность и бюрократия у нас. Страшно представить, сколько людей тратят месяцы на неверное лечение в связи с неверным диаонозом, потом по два месяца ждут очередь к специалисту, потом ждут результаты биопсии, и ещё три месяца ждут в очереди к онкологу. Ладно, когда кишечные опухоли могут развиваться годами не метастазируя. А есть крайне агрессивные опухоли, которые из горошинки дают дальние метастазы за считанные месяцы. А это для человека приговор за потерянное впустую время.
Отправить комментарий